Novavax ist ein in Maryland ansässiges Biotechnologieunternehmen, das einen traditionellen Ansatz zur Entwicklung eines Impfstoffs gegen die Coronavirus-Krankheit 2019 (COVID-19) verfolgt. Das Unternehmen startete im September in Großbritannien eine Phase-3-Studie mit seinem Impfstoffkandidaten NVX-CoV2373 und im Dezember eine zweite Phase-3-Studie in den USA und in Mexiko. An diesen beiden Studien im Spätstadium werden insgesamt etwa 45.000 Teilnehmer teilnehmen.
Während Novavax damit hinter seinen Konkurrenten zurückbleibt, sind die ersten Ergebnisse seiner Impfstoffversuche vielversprechend.
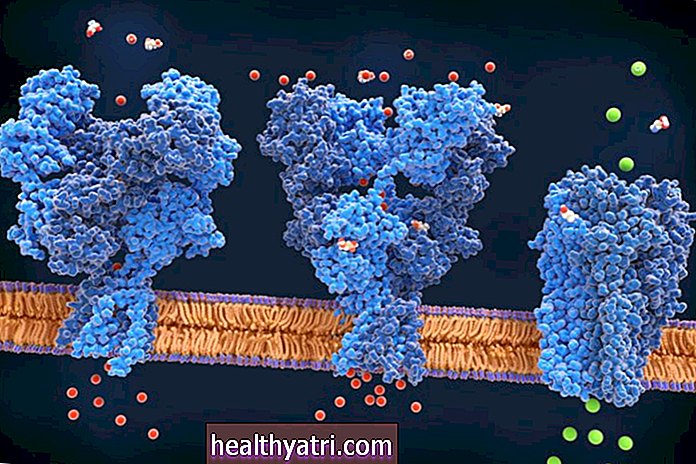
zoranm / Getty ImagesWie es funktioniert
Der Novavax-Impfstoff verwendet ein maßgeschneidertes Spike-Protein, das das natürliche Spike-Protein des neuartigen Coronavirus nachahmt. Novavax hat jahrelang an der Entwicklung seiner rekombinanten Nanopartikel-Technologie gearbeitet und im Frühjahr den ersten COVID-19-Impfstoff mit dieser Methode entwickelt. Bis zum Sommer zeigten frühe klinische Studien, dass der Impfstoff sicher zu sein schien, und fortgeschrittenere Studien traten in den USA und anderen Ländern in die Planungsphase ein.
Der Impfstoff mit zwei Dosen führt ein Protein ein, das eine Antikörperantwort auslöst, die die Fähigkeit des zukünftigen Coronavirus blockiert, sich an menschliche Zellen zu binden, und eine Infektion verhindert. Das Protein wird mit dem Matrix-M-Adjuvans von Novavax kombiniert, das für die Verstärkung der durch das Proteinantigen ausgelösten Immunantwort wichtig ist.
Wie effektiv ist es?
Frühe von Novavax veröffentlichte Ergebnisse von Impfstoffversuchen zeigten eine starke Antikörperantwort auf den Impfstoff bei Tieren. Bis August 2020 zeigten frühe Studien am Menschen starke Antikörperreaktionen ohne schwerwiegende unerwünschte Ereignisse und mit wenigen Nebenwirkungen.
Ende Januar gab Novavax bekannt, dass eine vorläufige Analyse der Daten aus seiner Phase-3-Studie in Großbritannien ergab, dass der Impfstoff zu 89,3% wirksam war und Schutz vor der britischen Variante B.1.1.7 beinhaltete. Das Unternehmen gab außerdem bekannt, dass der Impfstoff in einer klinischen Phase-2b-Studie in Südafrika zu 60% wirksam war und Schutz vor der südafrikanischen Variante B.1.351 beinhaltete.
Ergebnisse aller klinischen Studien im Spätstadium werden für 2021 erwartet.
In der Novavax-Studie werden die Teilnehmer nicht direkt dem Virus ausgesetzt sein, sondern die Forscher werden einen natürlichen Infektionsansatz verwenden. Die Herausforderung wird dann darin bestehen, festzustellen, ob der Impfstoff oder andere Schutzmaßnahmen wie Maskierung oder soziale Distanzierung den größten Schutz bieten.
Wann wird es verfügbar sein?
Der Impfstoffkandidat von Novavax stößt auf großes Interesse, da Daten aus frühen Tierstudien zeigten, dass er die Replikation des Coronavirus in Nasengängen hochwirksam verhindert. Dies ist eine wichtige Entwicklung für COVID-Impfstoffe, da er sowohl die Infektions- als auch die Übertragungsrate senken kann . Dies wurde jedoch in Humanstudien noch nicht nachgewiesen.
Novavax ist jedoch in Bezug auf klinische Studien hinter seinen Konkurrenten zurückgeblieben. Selbst wenn es in Studien weiterhin gut läuft, ist der Impfstoff möglicherweise erst Ende 2021 verfügbar. Das Unternehmen hat noch keine Schätzungen zu den Verteilungsterminen veröffentlicht. Das Unternehmen selbst steht auch vor einer großen Herausforderung, da 2019 für Novavax ein schwieriges Jahr war.WissenschaftDas Magazin berichtete, dass das Unternehmen einige seiner Produktionsanlagen verkauft und sich bei der Herstellung vieler seiner Impfstoffe auf mehr Auftragnehmer verlassen muss. Dies kann zu einer Verzögerung der Produktion führen.
Über den Preis des Impfstoffs liegen noch keine Informationen vor.
COVID-19-Impfstoffe: Bleiben Sie auf dem Laufenden, welche Impfstoffe verfügbar sind, wer sie erhalten kann und wie sicher sie sind.
Wer kann den Novavax-Impfstoff bekommen?
Wie andere COVID-19-Impfstoffkandidaten wurde der Novavax-Impfstoff bei Erwachsenen ab 18 Jahren getestet. Das Unternehmen hat keine Aktualisierungen zu Studien bei Kindern und Jugendlichen bereitgestellt. Es wurden noch keine Informationen zu Bedenken für bestimmte Gruppen bereitgestellt.
Unabhängig von der Bevölkerungsgruppe der Studiengruppen wird die Entscheidung, wer COVID-Impfstoffe erhalten kann, weitgehend von der FDA (Food and Drug Administration) getroffen. Die Berechtigung während der Verteilung wird dann auf staatlicher Ebene und von den Zentren für die Kontrolle und Prävention von Krankheiten (CDC) festgelegt.
Die CDC führt die Impfbemühungen an, und alle Bestellungen des COVID-19-Impfstoffs, unabhängig vom Hersteller, werden über die Agentur abgewickelt. Die CDC überwacht auch die Verteilung von Impfstoffen. Der Beratende Ausschuss für Immunisierungspraktiken (ACIP) der CDC hat Empfehlungen zur Priorisierung der Impfstoffversorgung abgegeben.
Beschäftigte im Gesundheitswesen und Menschen, die in Langzeitpflegeeinrichtungen leben, erhielten als erste die zugelassenen COVID-19-Impfstoffe. Laut CDC gibt es in den Vereinigten Staaten mehr als 18 Millionen Beschäftigte im Gesundheitswesen und etwa 1,3 Millionen Amerikaner, die in Langzeitpflegeeinrichtungen leben. Jede dieser Personen müsste zwei Dosen der zugelassenen Impfstoffe erhalten bisher.
Die CDC schätzt, dass es einige Monate dauern wird, bis das Angebot an Impfstoffen die Nachfrage befriedigt. Hinweise dazu, wer den Impfstoff erhält und wann, wird entschieden, sobald Lieferungen verfügbar sind. Allein in den Vereinigten Staaten leben etwa 330 Millionen Menschen - was bedeutet, dass fast 700 Millionen Impfstoffdosen erforderlich sind, um ganz Amerika zu impfen, wenn andere Impfstoffe einer Dosis von zwei Impfstoffen folgen.
Obwohl nur wenige Informationen darüber verfügbar sind, wann jeder die Impfstoffe erhalten wird und wo er sie erhalten kann, werden die staatlichen und lokalen Gesundheitsbehörden die Bemühungen koordinieren, die Dosen der Impfstoffe zu verteilen, sobald sie verfügbar sind. Der Impfstoff sollte sowohl in Arztpraxen als auch in Einzelhandelsgeschäften wie Apotheken erhältlich sein, die andere Impfstoffe verabreichen.
Sobald der Impfstoff verfügbar ist, sind alle von der US-Regierung gekauften Dosen für die Bürger kostenlos. Während der Impfstoff selbst kostenlos ist, kann die Einrichtung oder Agentur, die den Impfstoff anbietet, eine Gebühr für die Verabreichung erheben. Es wird erwartet, dass öffentliche Gesundheitsprogramme und Versicherungspläne den Patienten die mit der COVID-19-Impfung verbundenen Kosten erstatten, es wurden jedoch noch keine Informationen zur Verfügung gestellt.
Nebenwirkungen und unerwünschte Ereignisse
In frühen Studien mit dem Novavax-Impfstoff wurden keine schwerwiegenden unerwünschten Ereignisse gemeldet. Weitere Informationen werden jedoch verfügbar sein, nachdem die Ergebnisse der Studien im Spätstadium veröffentlicht wurden. In Phase 3 traten unerwünschte Ereignisse "in geringen Mengen auf und waren zwischen Impfstoff- und Placebogruppen ausgewogen". nach Novavax.
Finanzierung und Entwicklung
Novavax hat weltweit mehr als 2 Milliarden US-Dollar für seine Bemühungen zur Entwicklung eines COVID-19-Impfstoffs erhalten, 1,6 Milliarden US-Dollar allein von der US-Regierung. Die US-Mittel wurden im Rahmen der Operation Warp Speed und von der Biomedical Advanced Research and Development Authority (BARDA) bereitgestellt. BARDA ist ein Programm, das dem US-amerikanischen Gesundheitsministerium untersteht. Dieses Programm und Operation Warp Speed haben versucht zu beschleunigen, wie schnell Impfstoffe zur Bekämpfung von COVID-19 entwickelt und zur Verwendung zugelassen werden können.



.jpg)






.jpg)










-works.jpg)
