Dex Images / Getty Images
Die zentralen Thesen
- Die FDA hat eine Kombination von Bamlanivimab und Eesevimab zur Behandlung von COVID-19 bei Patienten zugelassen, bei denen ein hohes Risiko für die Entwicklung von Komplikationen besteht.
- Die neue Kombination "reduzierte" das Risiko schwerer Komplikationen in einer klinischen Studie "signifikant".
- Die FDA hat zuvor Bamlanivimab allein zur Anwendung zugelassen.
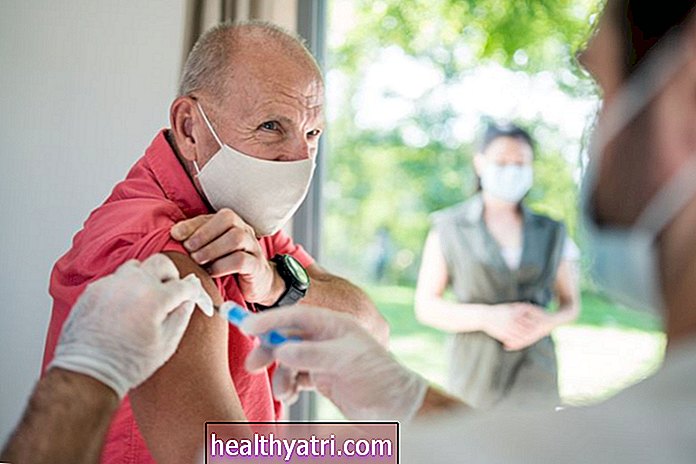
Die Food and Drug Administration (FDA) hat eine zweite monoklonale Antikörpertherapie zur Behandlung von Patienten mit COVID-19 zugelassen. Die Agentur erteilte den Arzneimitteln Bamlanivimab und Eesevimab, die zusammen zur Behandlung von leichtem bis mittelschwerem COVID-19 bei Personen ab 12 Jahren angewendet werden, bei denen ein hohes Risiko für die Entwicklung von schwerem COVID-19 besteht, eine Genehmigung zur Verwendung in Notfällen (EUA).
Eine klinische Studie ergab, dass eine einzelne intravenöse Infusion von Bamlanivimab und Eesevimab das Risiko einer Krankenhauseinweisung und des Todes durch COVID-19 während der 29-tägigen Nachbeobachtungszeit im Vergleich zu einem Placebo bei Patienten mit dem Virus, bei denen ein hohes Risiko bestand, „signifikant verringerte“ Fortschreiten zu schwerer Krankheit.
An der Studie nahmen 1.035 nicht hospitalisierte Erwachsene mit leichten bis mittelschweren COVID-19-Symptomen teil, bei denen ein hohes Risiko für das Fortschreiten von schwerem COVID-19 bestand, und gaben ihnen entweder eine einmalige Infusion von 2.800 Milligramm Bamlanivimab und Eesevimab oder ein Placebo. Die Forscher fanden heraus, dass 36 Patienten (7%), die das Placebo erhielten, ins Krankenhaus eingeliefert wurden oder starben, verglichen mit 11 (2%), die mit der Kombinationstherapie behandelt wurden, was einer Reduktion von 70% entspricht. Es gab 10 Todesfälle und alle waren Patienten in der Placebogruppe.
Die FDA gibt an, dass Menschen mit „schweren, lang anhaltenden (chronischen) Erkrankungen“ wie Herzerkrankungen, Lungenerkrankungen und Diabetes „ein höheres Risiko haben, wegen COVID-19 ins Krankenhaus eingeliefert zu werden“.
Dies ist nicht die erste Behandlung mit monoklonalen Antikörpern, die von der FDA zugelassen wurde. Die Agentur gewährte allein im November eine EUA für Bamlanivimab.
Bamlanivimab "erwies sich als wirksam bei der Reduzierung der Krankenhausaufenthaltsraten bei Patienten mit hohem Risiko für ein Fortschreiten der Krankheit, wenn es zu Beginn der Krankheit angewendet wird", so Dr. Sunanda Gaur, Direktor des klinischen Forschungszentrums an der Rutgers Robert Wood Johnson Medical School in New Jersey. erzählt Verywell.
Gaur sagt, die Ergebnisse der Studie seien "vielversprechend", weist jedoch darauf hin, dass die vollständigen Daten noch nicht verfügbar sind. Dennoch, sagt sie, ist diese Kombination "potenziell wirksamer als Bamlanivimab allein gegeben".
Was dies für Sie bedeutet
Es ist immer eine gute Nachricht, wenn eine andere Behandlung für COVID-19 zugelassen ist. Wenn Sie jedoch keinen zugrunde liegenden Gesundheitszustand haben, ist es unwahrscheinlich, dass Ihnen diese Behandlung zur Verfügung steht, wenn Sie sich mit COVID-19 infizieren.
Wie funktioniert es?
Bamlanivimab ist eine monoklonale Antikörpertherapie, die direkt an Teile von Viren bindet, um zu verhindern, dass diese eine Person infizieren. Bamlanivimab zielt auf das Spike-Protein von SARS-CoV-2 ab, dem Virus, das COVID-19 verursacht. Es wurde entwickelt, um die Fähigkeit des Virus zu blockieren, menschliche Zellen anzulagern und in sie einzudringen. Die Behandlung erfolgt durch eine IV.
Etesevimab ist auch ein monoklonaler Antikörper, der an die Oberfläche des SARS-CoV-2-Spike-Proteinrezeptors bindet. Etesevimab wirkt ähnlich wie Bamlanivimab und wurde von derselben Firma, Eli Lilly, entwickelt.
Nicht jeder hat Anspruch auf diese Behandlung. Die FDA gibt an, dass nur Personen ab 12 Jahren, bei denen ein hohes Risiko für schwerwiegende Komplikationen des Virus besteht, die Behandlung erhalten können.
Bamlanivimab und Etevimab sind nicht für Patienten zugelassen, die im Krankenhaus sind oder aufgrund von COVID-19 eine Sauerstofftherapie benötigen. Monoklonale Antikörper wie Bamlanivimab und Eesevimab können bei diesen Patienten zu schlechteren Ergebnissen führen, insbesondere bei Patienten, die Sauerstoff mit hohem Durchfluss oder mechanische Beatmung benötigen.
Gemischte Gefühle
Während Ärzte die Nachrichten begrüßen, weisen einige darauf hin, dass viele auf dem Gebiet keine monoklonalen Antikörper verwendet haben. "Einige hatten in größeren klinischen Studien auf zusätzliche Beweise für die Wirksamkeit dieser Wirkstoffe gewartet", sagt Dr. Prathit Kulkarni, Assistenzprofessor für Medizin bei Infektionskrankheiten am Baylor College of Medicine in Texas, gegenüber Verywell.
Infolgedessen "gibt es einen allgemeinen Mangel an Wissen über monoklonale Antikörper in der medizinischen Gemeinschaft", sagt Dr. Richard Watkins, Arzt für Infektionskrankheiten und Professor für Innere Medizin an der Northeast Ohio Medical University, gegenüber Verywell. Und er fügt hinzu: "Viele Patienten haben noch nie von ihnen gehört."
Kulkarni stellt fest, dass die jüngste Notfallgenehmigung auf Ergebnissen einer größeren klinischen Phase-3-Studie basiert.
Die Behandlung selbst ist auch komplizierter als nur jemandem eine Pille zu verschreiben, sagt Watkins und bemerkt, dass "es Personalprobleme gibt, wenn es darum geht, die Infusionen in ambulanten Einrichtungen zu verabreichen".
Gaur stimmt zu. "Die Verabreichung ist logistisch schwierig, da eine Infusion erforderlich ist, die mehrere Stunden dauern kann", sagt sie. "Um Ärzte zu überzeugen, werden robustere Daten zum Nutzen dieses Ansatzes einer frühzeitigen Behandlung erforderlich sein."
Insgesamt sagt Watkins jedoch, dass die Genehmigung vielversprechend ist. "Ich bin froh, dass Ärzte jetzt eine weitere Therapie zur Bekämpfung von COVID-19 erhalten", sagt er.