Pool / Pool / Getty Images
Die zentralen Thesen
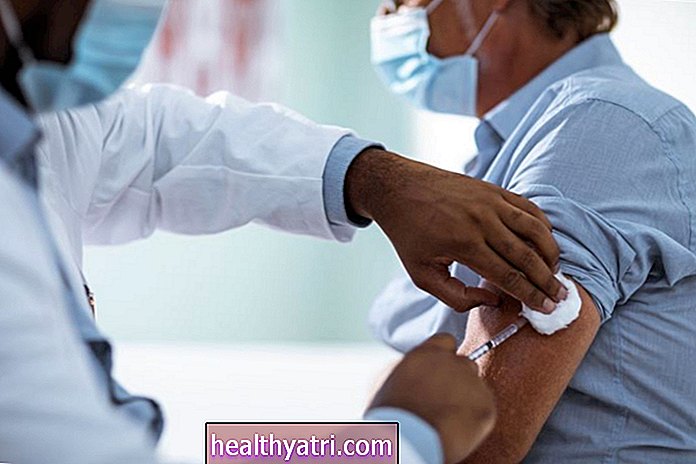
- Jeder, der 65 Jahre oder älter ist, kann jetzt den Impfstoff erhalten
- Personen unter 65 Jahren mit einem dokumentierten Gesundheitsproblem, das das Risiko von COVID-19 erhöht, sind jetzt ebenfalls berechtigt.
- Der Zeitplan für die zweite Dosis der derzeit verfügbaren Impfstoffe - 21 Tage nach der ersten für den Pfizer-Impfstoff; 28 Tage nach dem ersten für den Moderna-Impfstoff - bleiben Sie gleich.
- Die Staaten müssen Standorte und medizinisches Personal hinzufügen, um die zusätzlichen Dosen zu verwalten, die die Bundesregierung freigeben wird. Wenden Sie sich an Ihren Arzt, Ihr örtliches Gesundheitsamt oder rufen Sie 311 an, um herauszufinden, wo die Aufnahmen in Ihrer Nähe verfügbar sind.
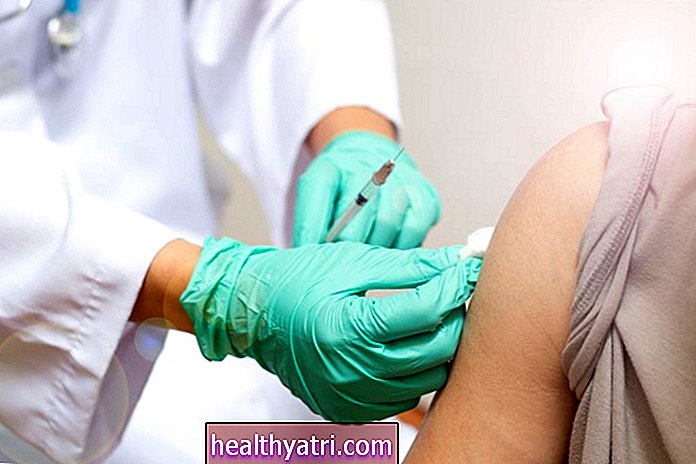
In einer Pressekonferenz am Dienstag, dem 12. Januar, legte der scheidende Sekretär für Gesundheit und menschliche Dienste (HHS), Alex Azar, neue Empfehlungen vor, um mehr Amerikaner früher gegen COVID-19 impfen zu lassen.
Die neuen Empfehlungen werden die Impfstoffdosen einer größeren Gruppe von Amerikanern leichter zugänglich machen:
- Jeder 65 und älter
- Menschen unter 65 Jahren mit dokumentierten chronischen Erkrankungen wie Bluthochdruck, Krebs und chronischen Lungenerkrankungen. und Herzerkrankungen.
Vor der Ankündigung folgten die meisten Staaten den Empfehlungen des Beratenden Ausschusses für Immunisierungspraktiken (ACIP) der Zentren für die Kontrolle und Prävention von Krankheiten (ACIP), während der anfänglichen Verteilungsphase nur Beschäftigte im Gesundheitswesen und Bewohner von Langzeitpflegeeinrichtungen zu impfen. Infolge dieser Änderung werden die Impfstellen um große öffentliche Veranstaltungsorte und mehr Einzelhandelsapotheken erweitert.
Anstatt Dosen zurückzuhalten, um sicherzustellen, dass diejenigen, die eine erste Impfung erhalten haben, ihre zweite Dosis rechtzeitig erhalten können, plant die Bundesregierung nun, die meisten verfügbaren Impfstoffdosen an die Bundesländer abzugeben.
"Jede Impfstoffdosis in einem Lagerhaus könnte einen weiteren Krankenhausaufenthalt oder Tod bedeuten", sagte Azar bei der Besprechung. Nach Angaben der Zentren für die Kontrolle und Prävention von Krankheiten (CDC) haben bis Montag etwas mehr als 10 Millionen Menschen mindestens eine Dosis eines COVID-19-Impfstoffs erhalten.
CDC-Direktor Robert Redfield, MD, sagte, die neuen Richtlinien stimmen mit früheren Planungen überein und die Regierung habe nie beabsichtigt, dass eine Impfphase endet, bevor eine andere beginnt.
Keine Änderung für den Dosierungsplan vorgesehen
Während der Pressekonferenz sagte Sekretär Azar, dass keine Änderungen hinsichtlich des Zeitpunkts für die zweite Dosis empfohlen werden. Die Empfehlung basiert weiterhin auf der Kennzeichnung gemäß der Notfallgenehmigung der Food and Drug Administration für Pfizer (21-tägige Trennung zwischen den Dosen) und Moderna (28-tägige Trennung zwischen den Dosen).
Azar sagte, sein Team werde den gewählten Präsidenten Biden über die neuen Empfehlungen informieren. Das Übergangsteam von Biden gab zuvor bekannt, dass der gewählte Präsident über Bemühungen sprechen wird, die Geschwindigkeit und das Tempo der Verteilung und Verabreichung von Impfstoffen an diesem Donnerstag zu erhöhen.
Die neuen Empfehlungen kommen daher, dass Fälle und Todesfälle in vielen Staaten weiter zunehmen. Bis zum 13. Januar gab es in den USA etwas mehr als 379.000 Todesfälle aufgrund von COVID-19.
„Dies ist der richtige Schritt, um Verschwendung zu vermeiden, schwere Krankheiten und Todesfälle zu vermeiden und das Gesundheitssystem zu entlasten“, so Leana Wen, MD, MSc, FAAEM, Notärztin und Gastprofessorin für Gesundheitspolitik und -management an der George Washington University, erzählt Verywell.
Am Ende des Briefings informierte Moncef Slaoui, Leiter der Operation Warp Speed des COVID-19-Impfstoffentwicklungsprogramms der Bundesregierung, die Reporter über das Tempo der COVID-19-Impfungen, die sich noch in klinischen Studien befinden:
- AstraZeneca: Voraussichtlich Anfang März eine Genehmigung für den Notfall beantragen.
- Novavax: Rekrutierung noch für klinische Studien. Ergebnisse werden Ende März / Anfang April erwartet.
- Sanofi: Voraussichtlich Mitte Februar mit den klinischen Studien der Phase 2b beginnen
Was dies für Sie bedeutet
In vielen Staaten gibt es inzwischen Registrierungswebsites für die COVID-19-Impfstoffe. Suchen Sie online oder rufen Sie 311 an, um herauszufinden, wie Sie sich anmelden können, insbesondere jetzt, wo mehr Menschen für den Impfstoff in Frage kommen.









.jpg)
-symptoms-and-treatment.jpg)